Cho các phương trình nhiệt hóa học sau:
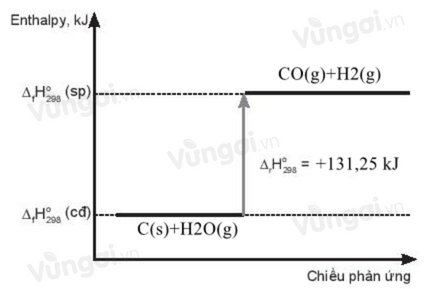
(1) C(s) + (H_2)O(g)->(((t^o)))CO(g) + (H_2)(g) ((Delta _r)H_(298)^0 = + 131,25kJ )
(2) (CuS(O_4)(aq) + Zn(s) -> ZnS(O_4)(aq) + Cu(s) ) ((Delta _r)H_(298)^0 = - 231,04kJ )
(3) 2(C_2)(H_5)OH(l) + 3(O_2)(g)->(((t^o)))2C(O_2)(g) + 3(H_2)O(l) ((Delta _r)H_(298)^0 = - 1366,89kJ )
(4) C(H_4)(g) + (H_2)O(l)->(((t^o)))CO(g) + 3(H_2)(g) ((Delta _r)H_(298)^0 = + 250kJ )
(5) (CaC(O_3)(s) -> CaO(s) + C(O_2)(g) ) ((Delta _r)H_(298)^0 = + 178,29kJ )
Số phản ứng tỏa nhiệt và phản ứng thu nhiệt lần lượt là
Câu 145710 Thông hiểu
Cho các phương trình nhiệt hóa học sau:
(1) C(s)+H2O(g)to→CO(g)+H2(g) ΔrH0298=+131,25kJ
(2) CuSO4(aq)+Zn(s)→ZnSO4(aq)+Cu(s) ΔrH0298=−231,04kJ
(3) 2C2H5OH(l)+3O2(g)to→2CO2(g)+3H2O(l) ΔrH0298=−1366,89kJ
(4) CH4(g)+H2O(l)to→CO(g)+3H2(g) ΔrH0298=+250kJ
(5) CaCO3(s)→CaO(s)+CO2(g) ΔrH0298=+178,29kJ
Số phản ứng tỏa nhiệt và phản ứng thu nhiệt lần lượt là
Đáp án đúng: a
Phương pháp giải
ΔrH>0: phản ứng thu nhiệt
ΔrH<0: phản ứng tỏa nhiệt
Xem lời giải
Lời giải của GV Vungoi.vn
Phản ứng thu nhiệt: (1), (4), (5)
Phản ứng tỏa nhiệt: (2), (3)
Đáp án cần chọn là: a